ГОСТ ISO 20633-2018
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
СМЕСИ АДАПТИРОВАННЫЕ ДЛЯ ИСКУССТВЕННОГО ВСКАРМЛИВАНИЯ ДЕТЕЙ РАННЕГО ВОЗРАСТА И СМЕСИ ДЛЯ ЭНТЕРАЛЬНОГО ПИТАНИЯ ВЗРОСЛЫХ
Определение содержания витамина Е и витамина А с помощью нормально-фазовой высокоэффективной жидкостной хроматографии
Infant formula and adult nutritionals. Determination of vitamin E and vitamin A by normal phase high performance liquid chromatography
МКС 67.050
Дата введения 2019-09-01
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-2015 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2015 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены"
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным бюджетным учреждением науки "Федеральный исследовательский центр питания, биотехнологии и безопасности пищи" (ФГБУН "ФИЦ питания и биотехнологии") на основе собственного перевода на русский язык международного стандарта, указанного в пункте 5
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 30 мая 2018 г. N 109-П)
За принятие проголосовали:
Краткое наименование страны | Код страны | Сокращенное наименование национального органа по стандартизации |
Беларусь | BY | Госстандарт Республики Беларусь |
Киргизия | KG | Кыргызстандарт |
Молдова | MD | Институт стандартизации Молдовы |
Россия | RU | Росстандарт |
Узбекистан | UZ | Узстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 22 августа 2018 г. N 514-ст межгосударственный стандарт ГОСТ ISO 20633-2018 введен в действие в качестве национального стандарта Российской Федерации с 1 сентября 2019 г.
5 Настоящий стандарт идентичен международному стандарту ISO 20633:2015* "Смеси адаптированные для искусственного вскармливания детей раннего возраста и смеси для энтерального питания взрослых. Определение содержания витамина Е и витамина А с помощью нормально-фазовой высокоэффективной жидкостной хроматографии" ("Infant formula and adult nutritionals - Determination of vitamin E and vitamin A by normal phase high performance liquid chromatography", IDT)
________________
* Доступ к международным и зарубежным документам, упомянутым в тексте, можно получить, обратившись в Службу поддержки пользователей. - .
6 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
1 Область применения
Настоящий стандарт устанавливает метод одновременного количественного определения витамина Е (-токоферола и
-токоферола ацетата) и витамина А (13-цис- и полного транс-изомера ретинола пальмитата и ретинола ацетата) в адаптированных смесях для искусственного вскармливания детей раннего возраста и в смесях для энтерального питания взрослых (порошкообразные смеси, готовые к употреблению жидкости и жидкие концентраты).
Ретинол не используется для обогащения пищевых продуктов, и поэтому стандарт не распространяется на его определение. Массовая доля ретинола, естественно присутствующего в продуктах, незначительна.
Настоящий стандарт не распространяется на определение стереоизомеров витамина Е--токоферола и
-токоферола ацетата по отдельности.
2 Термины и определения
2.1 смеси для энтерального питания взрослых (adult nutritional): Полноценный в питательном отношении специализированный пищевой продукт, изготовленный из молока, сои, риса, молочной сыворотки, гидролизата белка, крахмала и аминокислот в любом сочетании, содержащий или не содержащий интактный белок, употребляемый в жидком виде; может являться единственным источником питания.
2.2 смеси адаптированные для искусственного вскармливания детей раннего возраста (infant formula): Заменитель грудного молока*, специально изготовленный для удовлетворения естественной потребности в питании младенцев в течение первых месяцев жизни до введения прикорма.
________________
* Термин в соответствии с ТР ТС 021/2011.
Примечание - Определение термина 2.2**.
________________
** Определение термина 2.2 взято из Codex Standard 72-1981.
3 Сущность метода
Для гидролиза гидрофильного внешнего слоя жировых мицелл в воде, присутствующих в анализируемой пробе образца, изготовленного на основе молока или сои, используют протеолитический фермент папаин. Затем гидрофобные компоненты мицелл количественно извлекают однократной экстракцией изооктаном. Экстракт анализируют методом нормально-фазовой ВЭЖХ, используя аналитическую колонку и градиентное элюирование. Количественное определение -токоферола и
-токоферола ацетата проводят с флуоресцентным детектированием при длине волны возбуждения 280 нм и длине волны эмиссии 310 нм. Ретинола пальмитат (цис- и транс-) и ретинола ацетат (цис- и транс-) количественно определяют с использованием УФ-детектирования при 325 нм.
4 Реактивы и материалы
Для проведения анализа при отсутствии особо оговоренных условий используют только реактивы гарантированной аналитической чистоты и дистиллированную или деминерализованную воду или аналогичную по чистоте воду.
4.1 Метил-трет-бутиловый эфир (МТБЭ) для ВЭЖХ.
4.2 n-Гексан для ВЭЖХ.
4.3 Этанол для ВЭЖХ.
4.4 Метанол для ВЭЖХ.
4.5 Изооктан (2,2,4-триметилпентан) для ВЭЖХ.
4.6 Фермент папаин [полученный из папайи (Carica papaya)], 3 ед./мг* или эквивалентный.
________________
* Например, фирмы Sigma 76220. Представлен пример доступной в коммерческой сети продукции. Данная информация приведена для удобства пользователей настоящего стандарта и не является рекламной поддержкой данной продукции. Допускается использование аналогичной продукции, обеспечивающей достоверные результаты.
4.7 Гидрохинон**.
________________
** Например, фирмы Sigma Н9003. Представлен пример доступной в коммерческой сети продукции. Данная информация приведена для удобства пользователей настоящего стандарта и не является рекламной поддержкой данной продукции. Допускается использование аналогичной продукции, обеспечивающей достоверные результаты.
4.8 Ледяная уксусная кислота, аналитически чистая.
4.9 Ацетат натрия, безводный.
4.10 Разбавленный раствор соляной кислоты
Разводят 100 см 36%-ного раствора соляной кислоты до 200 см
водой.
4.11 Раствор папаина массовой концентрации =20 г/дм
Растворяют 100 мг гидрохинона и 4 г безводного ацетата натрия в объеме около 80 см воды в мерной колбе вместимостью 100 см
(см. 5.11). рН раствора доводят до 5,0 добавлением разбавленного раствора соляной кислоты (см. 4.10). Добавляют 2 г папаина и объем доводят до метки водой. Раствор готовят в день использования.
4.12 Подкисленный раствор метанола
20 см ледяной уксусной кислоты добавляют к 1 дм
метанола и перемешивают. Раствор готовят в день использования.
4.13 Подвижная фаза А для ВЭЖХ
н-Гексан фильтруют и дегазируют в течение 15 мин с помощью ультразвуковой бани.
4.14 Подвижная фаза В для ВЭЖХ
Смешивают 750 см н-гексана и 250 см
метил-трет-бутилового эфира. Затем добавляют 3 см
метанола, фильтруют и дегазируют в течение 15 мин с помощью ультразвуковой бани.
4.15 Стандартные образцы сравнения
4.15.1 Ретинола пальмитат, первичный стандартный образец сравнения, содержащий антиоксидант (СAS 78-81-2).
4.15.2 Ретинола ацетат, первичный стандартный образец сравнения (CAS 127-47-9).
4.15.3 -Токоферола ацетат, первичный стандартный образец сравнения (CAS 7695-91-2).
4.15.4 -Токоферол, первичный стандартный образец сравнения (CAS 10191-41-0).
4.16 Основные растворы
4.16.1 Основной стандартный раствор ретинола пальмитата
Взвешивают около 70 мг ретинола пальмитата (см. 4.15.1) с точностью до 0,01 мг в мерную колбу вместимостью 50 см (см. 5.11), растворяют в изооктане и доводят до метки изооктаном (см. 4.5).
4.16.2 Основной стандартный раствор ретинола ацетата
Взвешивают около 35 мг ретинола ацетата (см. 4.15.2) с точностью до 0,01 мг в мерную колбу вместимостью 50 см (см. 5.11), растворяют в этаноле и доводят до метки этанолом (см. 4.3).
4.16.3 Основной стандартный раствор -токоферола ацетата
Взвешивают около 180 мг -токоферола ацетата (см. 4.15.3) с точностью до 0,01 мг в мерную колбу вместимостью 50 см
(см. 5.11), растворяют в изооктане и доводят до метки изооктаном (см. 4.5).
4.16.4 Основной стандартный раствор -токоферола
Взвешивают около 100 мг -токоферола (см. 4.15.4) с точностью до 0,01 мг в мерную колбу вместимостью 50 см
(см. 5.11), растворяют в изооктане и доводят до метки изооктаном (см. 4.5).
Примечание - Срок хранения приготовленных растворов - семь дней при температуре от 4 до 8°C.
4.16.5 Стандартный раствор смеси витаминов N 1
4 см основного стандартного раствора ретинола пальмитата (см. 4.16.1), 4 см
основного стандартного раствора ретинола ацетата (см. 4.16.2), 7 см
основного стандартного раствора
-токоферола ацетата (см. 4.16.3) и 20 см
основного стандартного раствора
-токоферола (см. 4.16.4) переносят пипеткой в мерную колбу вместимостью 50 см
(см. 5.11) и доводят до метки изооктаном. Раствор готовят в день использования.
4.16.6 Стандартный раствор смеси витаминов N 2
8 см стандартного раствора N 1 (см. 4.16.5) переносят пипеткой в мерную колбу вместимостью 100 см
(см. 5.11) и доводят до метки изооктаном. Раствор готовят в день использования.
4.16.7 Градуировочные растворы
В мерные колбы вместимостью 50 см (см. 5.11) переносят пипеткой 0,5, 2,0; 4,0; 8,0; 16,0 и 32,0 см
стандартного раствора смеси витаминов N 2 (см. 4.16.6) и доводят до метки изооктаном. Эти растворы используют для построения градуировочного графика по нескольким точкам. Раствор готовят в день использования.
Примечание - Для текущего контроля градуировочного графика и в зависимости от диапазона концентрации определяемых витаминов в исследуемых образцах можно использовать три или четыре градуировочных раствора, минимальная и максимальная массовая концентрация витаминов которых находятся внутри диапазона концентраций 6 точечного градуировочного графика.
4.17 Определение чистоты стандартных растворов
4.17.1 Спектрофотометрическое определение чистоты стандартного раствора ретинола пальмитата
1 см стандартного раствора ретинола пальмитата (см. 4.16.1) переносят пипеткой в мерную колбу вместимостью 100 см
(см. 5.11) и доводят до метки этанолом. Измеряют оптическую плотность раствора в кварцевой кювете с толщиной поглощающего слоя 1 см при длине волны 325 нм относительно этанола. Измерение повторяют два раза, каждый раз заполняя кювету раствором. Рассчитывают среднее величины оптической плотности. Рассчитывают чистоту ретинола пальмитата
в виде десятичных долей по формуле
![]() , (1)
, (1)
где А - среднее величины оптической плотности;
975 - коэффициент поглощения ретинола пальмитата при 325 нм (см. [1]);
- масса образца сравнения, мг.
4.17.2 Спектрофотометрическое определение чистоты стандартного раствора ретинола ацетата
1 см стандартного раствора ретинола ацетата (см. 4.16.2) переносят пипеткой в мерную колбу вместимостью 100 см
(см. 5.11) и доводят до метки этанолом. Измеряют оптическую плотность раствора в кварцевой кювете с толщиной поглощающего слоя 1 см при длине волны 325 нм относительно этанола. Измерение повторяют два раза, каждый раз заполняя кювету раствором. Рассчитывают среднее величины оптической плотности. Рассчитывают чистоту ретинола ацетата
в виде десятичных долей по формуле
![]() , (2)
, (2)
где А - среднее величины оптической плотности;
1560 - коэффициент поглощения ретинола ацетата при 325 нм (см. [1]);
- масса образца сравнения, мг.
4.17.3 Спектрофотометрическое определение чистоты стандартного раствора -токоферола ацетата
3 см стандартного раствора
-токоферола ацетата (см. 4.16.3) переносят пипеткой в мерную колбу вместимостью 100 см
(см. 5.11) и доводят до метки этанолом. Измеряют оптическую плотность раствора в кварцевой кювете с толщиной поглощающего слоя 1 см при длине волны 284 нм относительно этанола. Измерение повторяют два раза, каждый раз заполняя кювету раствором. Рассчитывают среднее величины оптической плотности. Рассчитывают чистоту
-токоферола ацетата
в виде десятичных долей по формуле
![]() , (3)
, (3)
где А - среднее величины оптической плотности;
43,6 - коэффициент поглощения -токоферола ацетата при 284 нм (см. [1]);
- масса образца сравнения, мг.
4.17.4 Спектрофотометрическое определение чистоты стандартного раствора -токоферола
3 см стандартного раствора
-токоферола (см. 4.16.4) переносят пипеткой в мерную колбу вместимостью 100 см
(см. 5.11) и доводят до метки этанолом. Измеряют оптическую плотность раствора в кварцевой кювете с толщиной поглощающего слоя 1 см при длине волны 292 нм относительно этанола. Измерение повторяют два раза, каждый раз заполняя кювету раствором. Рассчитывают среднее величины оптической плотности. Рассчитывают чистоту
-токоферола
в виде десятичных долей по формуле
![]() , (4)
, (4)
где А - среднее величины оптической плотности;
75,8 - коэффициент поглощения -токоферола при 292 нм (см. [1]);
- масса образца сравнения, мг.
4.17.5 Хроматографическое определение чистоты стандартных растворов
Готовят ряд стандартных растворов согласно следующей процедуре.
В четыре мерные колбы вместимостью 100 см (см. 5.11) переносят пипеткой по 1 см
стандартного раствора ретинола пальмитата (см. 4.16.1), ретинола ацетата (см. 4.16.2),
-токоферола ацетата (см. 4.16.3),
-токоферола (см. 4.16.4) и каждый раствор доводят до метки изооктаном. На каждой колбе отмечают наименование стандарта.
В четыре флакона автосамплера вместимостью 2 см переносят автоматическим дозатором 60 мм
раствора ретинола пальмитата, 30 мм
ретинола ацетата, 100 мм
-токоферола ацетата и 400 мм
-токоферола. Добавляют в каждый флакон изооктан до 2 см
.
Растворы во флаконах быстро перемешивают и проводят хроматографический анализ в соответствии с параметрами системы для ВЭЖХ (см. 6.2). Детектирование ретинола пальмитата и ретинола ацетата проводят при 325 нм. Детектирование ацетата -токоферола проводят при 284 нм,
-токоферола - при 292 нм.
Рассчитывают хроматографическую чистоту стандартов (СР) в виде десятичных долей после интегрирования всех пиков на хроматограмме каждого стандарта по формуле
![]() . (5)
. (5)
При расчете чистоты стандарта ретинола пальмитата (ацетата) учитывают только площадь транс-пиков.
4.17.6 Расчет концентрации градуировочных растворов стандартных образцов сравнения
Рассчитывают концентрацию, , каждого витамина в градуировочном стандартном растворе ретинола пальмитата (RP) и ретинола ацетата (RA) в мкг/см
,
-токоферола (Т) и
-токоферола ацетата (ТА), мг/дм
, по формулам:
![]() , (6)
, (6)
![]() , (7)
, (7)
![]() , (8)
, (8)
![]() , (9)
, (9)
где - объем градуировочного раствора соответственно 0,5; 2,0; 4,0; 8,0; 16,0 и 32,0 см
;
- масса стандартного образца сравнения, мг;
- спектрофотометрическая чистота;
- хроматографическая чистота;
1000 - коэффициент пересчета мг/см в мкг/см
.
5 Средства измерений, вспомогательное оборудование и материалы
При проведении испытания используют обычное лабораторное оборудование, в частности следующее.
5.1 Система для ВЭЖХ, состоящая из насоса, автоматического устройства для ввода проб, программируемого УФ-детектора для определения витамина А при длине волны детектирования 325 нм и флуоресцентного детектора для определения витамина Е при длине волны возбуждения 280 нм и длине волны эмиссии 310 нм.
5.2 Колонка для ВЭЖХ* аналитическая, заполненная нормально-фазовым сорбентом, или эквивалентная.
________________
* Например, Agilent Zorbax® NH2 (5 мкм, 1504,6 мм). Представлен пример доступной в коммерческой сети продукции. Данная информация приведена для удобства пользователей настоящего стандарта и не является рекламной поддержкой данной продукции. Допускается использование аналогичной продукции, обеспечивающей достоверные результаты.
5.3 Баня водяная, обеспечивающая поддержание температуры (37±2)°С.
5.4 Центрифуга с адапторами для пробирок вместимостью 50 см, обеспечивающая центрифугирование при 4000 об./мин.
5.5 Спектрофотометр, пригодный для измерений оптической плотности в ультрафиолетовом и видимом спектральном диапазоне в комплекте с 1 см кварцевой кюветой.
5.6 Весы аналитические, обеспечивающие точность взвешивания до четвертого десятичного знака после запятой.
5.7 Флаконы для автоматического ввода пробы в систему для ВЭЖХ из темного стекла вместимостью 2 см с пластиковой крышкой и пломбой из политетрафторэтилена (ПТФЭ).
5.8 Пробирки центрифужные вместимостью 50 см.
5.9 Встряхиватель механический лабораторный для пробирок.
5.10 Баня ультразвуковая.
5.11 Колбы мерные вместимостью 50 и 100 см.
5.12 Устройство для фильтрования под вакуумом через фильтр из нейлона с диаметром пор 0,45 мкм.
5.13 Колбы стеклянные лабораторные вместимостью 250 см, 1 и 2 дм
.
5.14 Пипетки и наконечники.
6 Проведение испытаний
6.1 Подготовка пробы
6.1.1 Общие положения
Если технологический процесс производства испытуемого образца неизвестен, пробоподготовку проводят в соответствии с 6.1.2.
6.1.2 Порошкообразные образцы, полученные смешиванием в сухом состоянии
Если образец получен смешиванием в сухом состоянии или является негомогенным, аккуратно взвешивают около 25 г () пробы в колбе вместимостью 250 см
(см. 5.13). Пробу разводят теплой водой (от 40 до 45°C), охлаждают и добавляют 200 г воды. Записывают конечную массу (
). Аккуратно из колбы отбирают и взвешивают около 5 г (
) восстановленного образца в центрифужной пробирке с завинчивающейся крышкой. Рассчитывают массу (эквивалентную сухому образцу)
по формуле
![]() . (10)
. (10)
6.1.3 Порошкообразные образцы, полученные смешиванием с увлажнением
Если образец является гомогенным или получен смешиванием с увлажнением, аккуратно взвешивают около 0,525 г пробы в центрифужной пробирке вместимостью 50 см с завинчивающейся крышкой. Добавляют 5 см
теплой воды с температурой около 40°C и встряхивают для растворения.
6.1.4 Жидкие образцы
Если образец является жидкой смесью, готовой к употреблению, или жидким концентратом, после тщательного перемешивания аккуратно взвешивают около 5 г пробы в центрифужной пробирке вместимостью 50 см с завинчивающейся крышкой.
6.1.5 Экстракция
К взвешенной пробе в центрифужной пробирке добавляют 5 см раствора папаина (см. 4.11) и тщательно перемешивают. Пробирку закрывают крышкой и нагревают на водяной бане при температуре (37±2)°C в течение 20-25 мин. По окончании нагревания пробирки снимают с водяной бани и охлаждают. Добавляют 20 см
подкисленного метанола (см. 4.12) и встряхивают в течение 10 мин, используя механический встряхиватель.
10 см изооктана переносят пипеткой в пробирку с анализируемым образцом. Пробирку аккуратно закрывают крышкой, чтобы предотвратить протекание, и встряхивают в течение 10 мин, используя механический встряхиватель. Затем центрифугируют в течение 10 мин при 4000 об./мин для получения прозрачного изооктанового слоя. Переносят аликвоту прозрачного изооктанового слоя во флакон из темного стекла, используемый для автоматического ввода в систему для ВЭЖХ-анализа.
6.2 ВЭЖХ-анализ
6.2.1 Общие положения
Для оптимального разделения и количественного определения рекомендуются:
- колонка аналитическая для ВЭЖХ*;
________________
* Например, Agilent Zorbax® NH2 (5 мкм, 1504,6 мм). Представлен пример доступной в коммерческой сети продукции. Данная информация приведена для удобства пользователей настоящего стандарта и не является рекламной поддержкой данной продукции. Допускается использование аналогичной продукции, обеспечивающей достоверные результаты.
- подвижная фаза А: n-гексан;
- подвижная фаза В: смесь 750 см n-гексана, 250 см
метил-трет-бутилового эфира, 3 см
метанола;
- скорость элюирования: 1,5 см/мин;
- вводимый объем: 50 мм;
- температура термостата колонки: (40±2)°C;
время хроматографического анализа: 20 мин.
Примеры хроматограмм - в приложении А.
6.2.2 Условия детектирования
Для спектрофотометрического (УФ) или диодно-матричного (ДАД) детектирования ретинола пальмитата или ретинола ацетата устанавливают длину волны 325 нм. Для флуоресцентного детектирования ацетата -токоферола или
-токоферола устанавливают длину волны возбуждения 280 нм, эмиссии - 310 нм.
6.2.3 Условия градиентного элюирования
Цикл насоса градиентного элюирования представлен в таблице 1.
Таблица 1 - Цикл насоса градиентного элюирования
Время, мин | Скорость потока, см | Подвижная фаза А, % | Подвижная фаза В, % |
0 | 1,5 | 95 | 5 |
3,0 | 1,5 | 95 | 5 |
12,0 | 1,5 | 5 | 95 |
14,0 | 1,5 | 5 | 95 |
15,0 | 1,5 | 95 | 5 |
20,0 | 1,5 | 95 | 5 |
7 Оценка пригодности условий хроматографического анализа
Условия хроматографического анализа должны быть подобраны таким образом, чтобы достигалось полное отделение пиков цис- от пиков транс-изомеров ретинола пальмитата (ацетата); т.е. коэффициент разделения соседних пиков стандартов должен быть более 1,5.
8 Обработка результатов
Пики цис- и транс-изомеров ретинола пальмитата и ретинола ацетата, -токоферола и
-токоферола ацетата на хроматограмме раствора пробы идентифицируют по совпадению значений времени удерживания с соответствующими значениями времени удерживания пиков витаминов на хроматограммах стандартных растворов при одинаковых хроматографических условиях.
Целью настоящего стандарта не является установление индивидуального вклада цис- и транс-изомеров пальмитата или ацетата ретинола в общую А-витаминную ценность.
При интегрировании пиков витамина А суммируют площади пиков 13-цис- и полного транс-изомеров ретинола пальмитата или ацетата в пересчете на транс-изомер.
Рассчитывают массовую концентрацию, w, в исследуемом образце (порошкообразном или жидком) ретинола пальмитата и ретинола ацетата в мкг/100 г, -токоферола или
-токоферола ацетата в мг/100 г по формуле
![]() , (11)
, (11)
где - площадь пика или высота пика ретинола пальмитата или ацетата (сумма площадей или высот пиков 13-цис- и полного транс-изомеров),
-токоферола или
-токоферола ацетата в растворе исследуемого образца;
- постоянная градуировочной кривой для каждого анализируемого вещества;
- наклон калибровочной кривой для каждого анализируемого вещества;
- использованный объем изооктана (здесь
=10 см
);
100 - коэффициент пересчета на 100 г образца;
- масса пробы (для жидкого образца) или масса сухого эквивалента в г (для порошкообразного образца).
Массовую долю витамина А пересчитывают на массовую долю ретинола по формуле
Витамин А в пересчете на ретинол (мкг/100 г)=(ретинола пальмитат
в мкг/100 г·0,55)+(ретинола ацетат в мкг/100 г·0,87). (12)
Массовую долю витамина Е пересчитывают на массовую долю -токоферола, используя стехиометрические соотношения:
- 1,10 мг -токоферола ацетата эквивалентен 1 мг
-токоферола и
- 1 мг=1,10 DL--токоферол (синтетический витамин Е; полностью рацемический
-токоферол).
Приложение А
(справочное)
Примеры хроматограмм
|
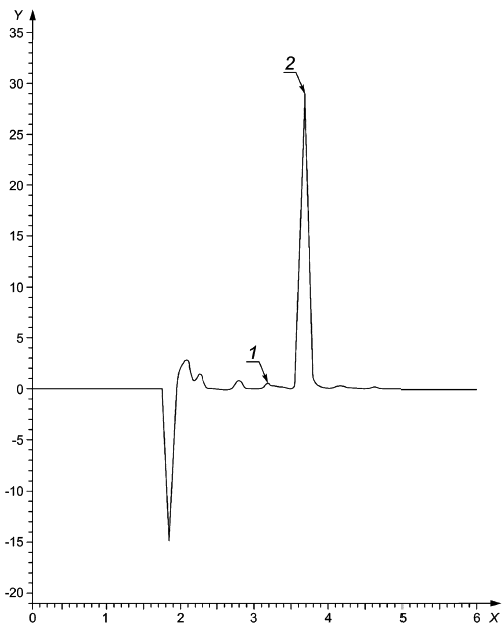
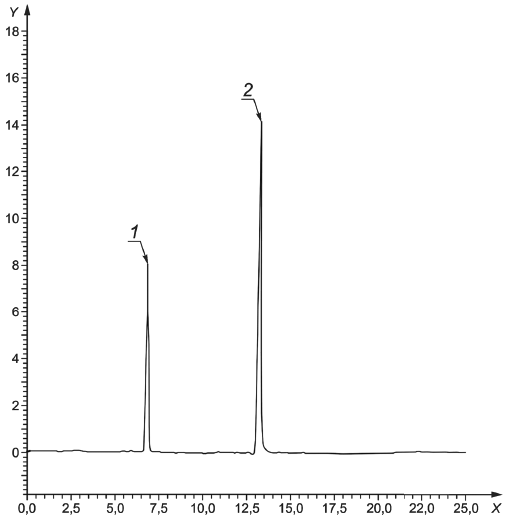
1 - 13-цис-изомер; 2 - транс-изомер; X - время, мин; Y - ед. опт. плотности (mAU)
Рисунок А.1 - Хроматограмма градуировочного раствора ретинола пальмитата
|
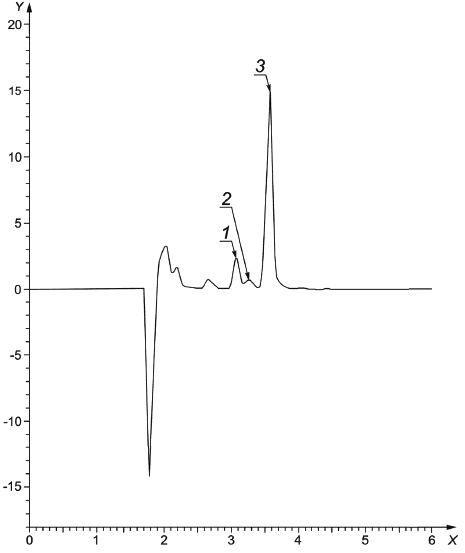
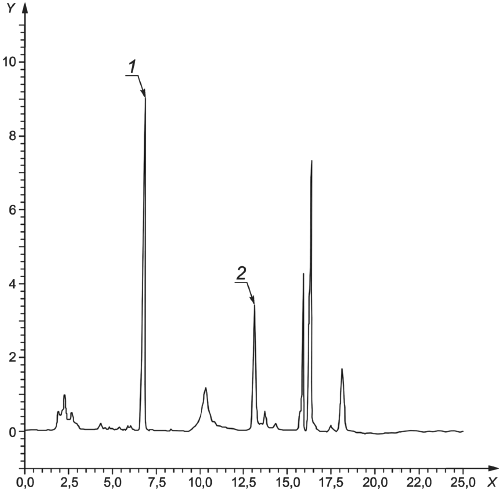
1 - 13-цис-изомер; 2 - цис-изомер; 3 - транс-изомер; X - время, мин; Y - ед. опт. плотности (mAU)
Рисунок А.2 - Хроматограмма ретинола пальмитата в исследуемом образце
|
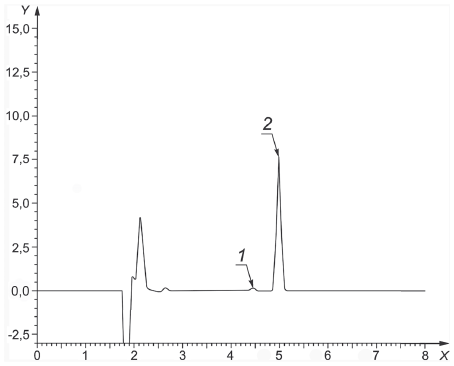
1 - 13-цис-изомер; 2 - транс-изомер; X - время, мин; Y - ед. опт. плотности (mAU)
Рисунок А.3 - Хроматограмма градуировочного раствора ретинола ацетата
|
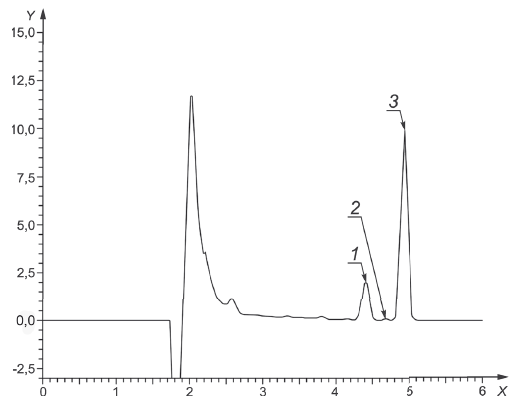
1 - 13-цис-изомер; 2 - цис-изомер; 3 - транс-изомер; X - время, мин; Y - ед. опт. плотности (mAU)
Рисунок А.4 - Хроматограмма ретинола ацетата в исследуемом образце
|
1 - -токоферола ацетат; 2 -
-токоферол; X - время, мин; Y - ед. опт. плотности (mAU)
Рисунок А.5 - Хроматограмма градуировочного раствора смеси -токоферола ацетата и
-токоферола
|
1 - ацетат -токоферола; 2 -
-токоферол; X - время, мин; Y - ед. опт. плотности (mAU)
Рисунок А.6 - Хроматограмма -токоферола ацетата и
-токоферола в исследуемом образце
Приложение В
(справочное)
Данные по прецизионности
Данные, приведенные в таблицах В.1, В.2 и В.3, были опубликованы в 2015 г. [2] и получены в результате проведения межлабораторных испытаний в соответствии с ISO 5725-2 [3] и Согласованным протоколом AOAC-IUPAC по проведению межлабораторных испытаний для оценки характеристик прецизионности методов анализа [4]. В основе процедуры проведения испытаний лежали требования, указанные в библиографических ссылках [5] и [6].
Дополнительную информацию по валидации метода анализа можно получить по адресу //standards.iso.org/iso/20633.
Таблица В.1 - Данные по прецизионности для ретинола ацетата (1 и 2
) и ретинола пальмитата (3
-8
) в пересчете на ретинол
Образцы | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
Год проведения межлабораторных испытаний | 2014 | 2014 | 2014 | 2014 | 2014 | 2014 | 2014 | 2014 |
Число лабораторий | 15 | 15 | 15 | 15 | 15 | 15 | 15 | 15 |
Число лабораторий, не отвечающих требованиям | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
Число лабораторий, оставшихся после исключения выбросов | 15 | 12 | 15 | 15 | 15 | 14 | 14 | 15 |
Число исключенных лабораторий | 0 | 3 | 0 | 0 | 0 | 1 | 1 | 0 |
Число принятых результатов | 30 | 24 | 30 | 30 | 30 | 28 | 28 | 30 |
Общее среднее х, мкг/100 г RTF | 46,34 | 67,39 | 6,49 | 47,55 | 62,56 | 66,58 | 57,34 | 48,35 |
Стандартное отклонение повторяемости | 7,69 | 1,55 | 0,21 | 7,50 | 4,28 | 0,75 | 0,61 | 7,31 |
Стандартное отклонение воспроизводимости | 10,48 | 8,04 | 0,52 | 10,33 | 6,04 | 4,33 | 4,13 | 7,86 |
Коэффициент вариации повторяемости | 16,60 | 2,30 | 3,26 | 15,78 | 6,84 | 1,13 | 1,06 | 15,13 |
Коэффициент вариации воспроизводимости | 22,61 | 11,93 | 8,02 | 21,73 | 9,66 | 6,51 | 7,20 | 16,25 |
Предел повторяемости | 21,54 | 4,34 | 0,59 | 21,01 | 11,98 | 2,10 | 1,70 | 20,48 |
Предел воспроизводимости | 29,34 | 22,52 | 1,46 | 28,92 | 16,91 | 12,13 | 11,56 | 21,99 |
Индекс воспроизводимости Горвица (HorRat R index) [7] | 1,25 | 0,69 | 0,33 | 1,20 | 0,56 | 0,38 | 0,41 | 0,91 |
Примечания 1 Результаты представлены в пересчете на мкг ретинола в 100 г RTF. 2 Результаты анализа SRM 1849а оказались ниже гарантированных значений, возможно, из-за несоответствующих условий хранения в ходе межлабораторных испытаний. Гарантированные значения [(7,68±0,23) мг/кг] были получены только в одной лаборатории, участвующей в совместных исследованиях образца [10]. | ||||||||
Таблица В.2 - Данные по прецизионности для витамина Е (-токоферола)
Образцы | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
Год проведения испытаний | 2014 | 2014 | 2014 | 2014 | 2014 | 2014 | 2014 | 2014 |
Число лабораторий | 15 | 15 | 15 | 15 | 15 | 15 | 15 | 15 |
Число лабораторий, не отвечающих требованиям | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
Число лабораторий, оставшихся после исключения выбросов | 14 | 11 | 14 | 14 | 14 | 13 | 14 | 14 |
Число исключенных лабораторий | 1 | 4 | 1 | 1 | 1 | 0 | 1 | 1 |
Число принятых результатов | 28 | 22 | 28 | 28 | 28 | 26 | 28 | 28 |
Общее среднее х, мкг/100 г RTF | 0,58 | 0,48 | 36,38 | 0,14 | 0,46 | 0,49 | 0,45 | 0,41 |
Стандартное отклонение повторяемости | 0,023 | 0,008 | 2,103 | 0,012 | 0,036 | 0,008 | 0,012 | 0,064 |
Стандартное отклонение воспроизводимости | 0,052 | 0,057 | 4,539 | 0,061 | 0,040 | 0,279 | 0,035 | 0,072 |
Коэффициент вариации повторяемости | 3,99 | 1,67 | 5,78 | 8,90 | 7,89 | 1,57 | 2,59 | 15,48 |
Коэффициент вариации воспроизводимости | 9,10 | 11,94 | 12,47 | 43,56 | 8,74 | 5,68 | 7,73 | 17,44 |
Предел повторяемости | 0,064 | 0,022 | 5,889 | 0,035 | 0,101 | 0,022 | 0,033 | 0,178 |
Предел воспроизводимости | 0,147 | 0,159 | 12,71 | 0,170 | 0,112 | 0,078 | 0,098 | 0,201 |
Индекс воспроизводимости Горвица R (HorRat R index) [7] | 0,930 | 0,920 | 1,870 | 2,180 | 0,680 | 0,440 | 0,600 | 1,340 |
| ||||||||
Таблица В.3 - Данные по прецизионности для витамина Е (-токоферола ацетата)
Образцы | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
Год проведения испытаний | 2014 | 2014 | 2014 | 2014 | 2014 | 2014 | 2014 | 2014 |
Число лабораторий | 15 | 15 | 15 | 15 | 15 | 15 | 15 | 15 |
Число лабораторий, не отвечающих требованиям | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
Число лабораторий, оставшихся после исключения выбросов | 14 | 15 | 14 | 13 | 14 | 13 | 13 | 15 |
Число исключенных лабораторий | 1 | 0 | 0 | 0 | 0 | 2 | 2 | 0 |
Число принятых результатов | 28 | 30 | 28 | 26 | 28 | 26 | 26 | 30 |
Общее среднее х, мкг/100 г RTF | 12,73 | 1,80 | 172,89 | 1,84 | 1,30 | 1,44 | 1,56 | 1,79 |
Стандартное отклонение повторяемости | 0,489 | 0,066 | 3,374 | 0,388 | 0,022 | 0,021 | 0,009 | 0,061 |
Стандартное отклонение воспроизводимости | 0,926 | 0,203 | 14,991 | 0,156 | 0,084 | 0,067 | 0,065 | 0,119 |
Коэффициент вариации повторяемости | 3,84 | 3,65 | 1,95 | 2,11 | 1,67 | 1,43 | 0,60 | 3,38 |
Коэффициент вариации воспроизводимости | 7,28 | 11,25 | 8,67 | 8,50 | 6,47 | 4,62 | 4,15 | 6,66 |
Предел повторяемости | 1,369 | 0,184 | 9,447 | 0,109 | 0,061 | 0,058 | 0,026 | 0,170 |
Предел воспроизводимости | 2,594 | 0,567 | 41,976 | 0,437 | 0,236 | 0,187 | 0,181 | 0,334 |
Индекс воспроизводимости Горвица R (HorRat R index) [7] | 0,330 | 1,070 | 0,580 | 0,810 | 0,580 | 0,42 | 0,380 | 0,630 |
| ||||||||
Приложение С
(справочное)
Сравнение методов АОАС 2012.10, EN 12822 и EN 12823-1
Для обеспечения сопоставимости данных, полученных методами EN 12822 [8], EN 12823-1 [9] и АОАС 2012.10 [10], были проанализированы одинаковые образцы. Для сравнения данные представлены в таблицах С.1 и С.2 и показаны на рисунках С.1 и С.2.
Таблица С.1 - Сравнение данных для витамина А
Образцы | АОАС 2012.10 | АОАС 2012.10 | EN 12823-1 | EN 12823-1 | EN 12823-1 |
n= от 11 до 15 лабораторий | n= от 11 до 15 лабораторий | Лаборатория 1 | Лаборатория 2 | Лаборатория 3 | |
мг/100 г RTF |
| мг/100 г RTF | мг/100 г RTF | мг/100 г RTF | |
Сухая смесь на основе молочного белка для энтерального питания взрослых | 46,34 | 22,61 | 48,29 | 50,84 | 38,07 |
Сухая адаптированная смесь для питания детей раннего возраста на основе частично гидролизованного белка соевых бобов | 67,39 | 11,93 | 74,93 | 76,92 | 51,28 |
SRM 1849а | 6,49 | 8,02 | 7,38 | 6,99 | 6,14 |
Сухая смесь с низким содержанием жира для энтерального питания взрослых | 47,55 | 21,73 | 62,16 | 61,16 | 53,61 |
Сухая адаптированная смесь для питания детей раннего возраста на основе белка соевых бобов | 62,56 | 9,66 | 69,71 | 72,59 | 58,16 |
Сухая адаптированная смесь для питания детей раннего возраста на основе молока | 66,58 | 6,51 | 70,60 | 69,71 | 60,27 |
Адаптированная смесь для питания детей раннего возраста на основе молока RTF | 57,34 | 7,20 | 68,35 | 67,00 | 58,00 |
Элементное питание для детей раннего возраста | 48,35 | 16,25 | 47,51 | 47,29 | 37,30 |
| |||||
На рисунке С.1 значения, полученные методом EN 12823-1 тремя участвующими лабораториями, нанесены на график против данных ±2 , полученных методом АОАС 2012.10 в ходе межлабораторных испытаний (MLT), в которых приняли участие от 11 до 15 лабораторий. Границы 2
включали 95% данных, полученных методом АОАС 2012.10.
|
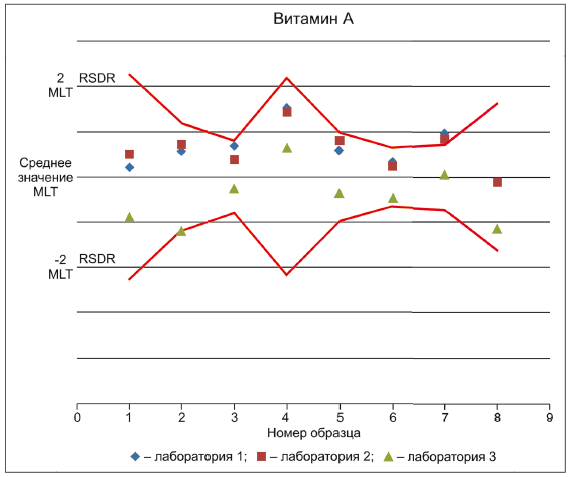
Примечание - Результаты, полученные методом EN 12823-1 тремя участвующими лабораториями, нанесены на график против данных ±2 , полученных методом АОАС 2012.10 в ходе межлабораторных испытаний (MLT), в которых приняли участие от 11 до 15 лабораторий. Данные трех участвующих лабораторий были стандартизованы относительно среднего значения, полученного методом АОАС 2012.10.
Рисунок С.1 - Сравнение методов определения витамина А
Таблица С.2 - Сравнение данных для витамина Е (-токоферола ацетат плюс
-токоферол в пересчете на
-токоферол)
Образцы | АОАС 2012.10 | АОАС 2012.10 | EN 12822 | EN 12822 | EN 12822 |
n= от 11 до 15 лабораторий | n= от 11 до 15 лабораторий | Лаборатория 1 | Лаборатория 2 | Лаборатория 3 | |
мг/100 г RTF |
| мг/100 г RTF | мг/100 г RTF | мг/100 г RTF | |
Сухая смесь на основе молочного белка для энтерального питания взрослых | 12,18 | 7,17 | 11,32 | - | 12,32 |
Сухая адаптированная смесь для питания детей раннего возраста на основе частично гидролизованного белка соевых бобов | 2,12 | 10,15 | 2,09 | 1,78 | 2,04 |
SRM 1849а | 193,90 | 3,91 | 186,50 | 125,00 | 191,00 |
Сухая смесь с низким содержанием жира для энтерального питания взрослых | 1,82 | 10,78 | 1,71 | 1,50 | 1,80 |
Сухая адаптированная смесь для питания детей раннего возраста на основе белка соевых бобов | 1,64 | 4,22 | 1,58 | 1,55 | 1,68 |
Сухая адаптированная смесь для питания детей раннего возраста на основе молока | 1,80 | 4,13 | 1,69 | 1,54 | 1,83 |
Адаптированная смесь для питания детей раннего возраста на основе молока RTF | 1,87 | 3,84 | 1,86 | 1,30 | 1,88 |
Элементное питание для детей раннего возраста | 1,77 | 5,55 | 1,81 | 1,70 | 2,03 |
| |||||
На рисунке С.2 данные испытаний, полученные методом EN 12822 тремя лабораториями, нанесены на график против данных ±2 , полученных методом АОАС 2012.10 в ходе межлабораторных испытаний (MLT), в которых приняли участие от 11 до 15 лабораторий. Границы 2
включали 95% данных, полученных с помощью метода валидации АОАС 2012.10.
|
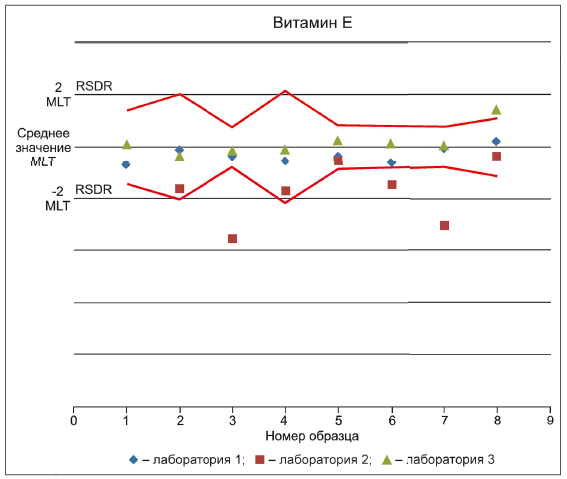
Примечание - На рисунке приведены результаты определения витамина Е (-токоферола ацетат плюс
-токоферол в пересчете на
-токоферол), полученные методом EN 12822 тремя лабораториями. Данные испытаний нанесены на график против данных 2
, полученных методом АОАС 2012.10 в ходе межлабораторных испытаний, в которых приняли участие от 11 до 15 лабораторий. Данные трех участвующих лабораторий были стандартизованы относительно среднего значения, полученного методом АОАС 2012.10.
Рисунок С.2 - Сравнение методов определения витамина Е
Библиография
[1] | Eitenmiller R.R., Landen Jr W.O. Vitamin Analysis for the Health and Food Sciences; CRC Press | |
[2] | ОМА 2012.10. Simultaneous Determination of 13-Cis and all-trans Vitamin A Palmitate (retinyl palmitate), Vitamin A Acetate (retinyl acetate), and Total Vitamin E ( | |
[3] | ISO 5725-2:1994 | Accuracy (trueness and precision) of measurement methods and results - Part 2: Basic method for the determination of repeatability and reproducibility of a standard measurement method [Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений]* |
________________ * Официальный перевод этого стандарта находится в Федеральном информационном фонде стандартов. | ||
[4] | AOAC INTERNATIONAL. AOAC Official Methods Program, Associate Referee's Manual on development, Study, Review, and Approval Process. Part IV AOAC Guidelines for Collaborative Studies, 1995, pp.23-51 | |
[5] | AOAC SMPR 2011.003. Standard Method Performance Requirements for Vitamin A in infant formula and Adult/Pediatric Nutritional formula | |
[6] | AOAC SMPR 2011.010. Standard Method Performance Requirements for Vitamin E in infant formula and Adult/Pediatric Nutritional formula | |
[7] | Thompson M. Recent Trends in Inter-Laboratory Precision at ppb and sub-ppb Concentrations in Relation to Fitness for Purpose Criteria in Proficiency Testing. Analyst (Lond.). 2000, 125, pp.385-386 | |
[8] | EN 12822:2014 | Foodstuffs - Determination of vitamin E by high performance liquid chromatography - Measurement of (Продукты пищевые. Определение витамина Е высокоэффективной жидкостной хроматографией. Измерение альфа-, бетта-, гамма- и дельта-токоферолов) |
[9] | EN 12823-1:2014 | Foodstuffs - Determination of vitamin A by high performance liquid chromatography - Part 1: Measurement of all-E-retinol and 13-Z-retinol (Продукты питания. Определение содержания витамина А методом жидкостной хроматографии высокого разрешения. Часть 1. Измерение содержания полного транс-ретинола и 13-Z-ретинола) |
[10] | J AOAC Int 2013, Sept-Oct; 96 (5): 1073-1081 - Simultaneous determination of 13-cis and all-trans vitamin A palmitate (retinyl palmitate), vitamin A acetate (retinyl acetate), and total vitamin E (alpha-tocopheryl and alpha-tocopheryl acetate) in infant formula and adult nutritionals by normal phase HPLC: first action 2012.10 | |
УДК 613.22:664:543.544.5.068.7:006.354 | МКС 67.050 |
Ключевые слова: смеси адаптированные для искусственного вскармливания детей раннего возраста, смеси для энтерального питания взрослых, ретинола пальмитат, ретинола ацетат, | |
Электронный текст документа
и сверен по:
, 2018