ГОСТ Р 51892-2002
(ИСО 11979-1-99)
Группа П46
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Имплантаты офтальмологические
ИНТРАОКУЛЯРНЫЕ ЛИНЗЫ
Часть 1
Термины и определения
Ophthalmic implants. Intraocular lenses. Part 1. Terms and definitions
ОКС 11.040.40
ОКП 94 8100
Дата введения 2003-01-01
Предисловие
1 РАЗРАБОТАН Государственным унитарным предприятием "Центр нормативно-информационных систем" ГП "ТКС-оптика ГОИ" совместно с испытательной лабораторией биологической безопасности медицинских изделий Федерального учреждения науки НИИ Трансплантации и искусственных органов
ВНЕСЕН Техническим комитетом ТК 296 "Оптика и оптические приборы"
2 ПРИНЯТ И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Госстандарта России от 17 мая 2002 г. N 191-ст
3 Настоящий стандарт содержит полный аутентичный текст международного стандарта ИСО 11979-1-99 "Имплантаты офтальмологические. Интраокулярные линзы. Часть 1. Термины и определения" с дополнительными требованиями, отражающими потребности экономики страны, выделенными в тексте стандарта курсивом
4 ВВЕДЕН ВПЕРВЫЕ
1 Область применения
Настоящий стандарт распространяется на интраокулярные линзы (далее - ИОЛ), предназначенные для оптической коррекции зрения путем хирургической имплантации внутрь глаза.
Стандарт устанавливает термины и определения, соблюдение которых должно обеспечиваться при разработке, производстве, поставке и сертификации ИОЛ.
Стандарт не распространяется на роговичные имплантаты и трансплантаты.
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на следующие стандарты:
ГОСТ Р ИСО 10993.1-99* Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования
______________
* На территории Российской Федерации с 01.07.2010 действует ГОСТ Р ИСО 10993-1-2009. - .
ГОСТ Р ИСО 10993.5-99 Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 5. Исследования на цитотоксичность: методы in vitro
ГОСТ Р ИСО 10993.6-99 Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 6. Исследование местного действия после имплантации
ГОСТ Р ИСО 10993.10-99* Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 10. Исследование раздражающего и сенсибилизирующего действия
______________
* На территории Российской Федерации с 01.09.2010 действует ГОСТ Р ИСО 10993-10-2009. - .
ГОСТ Р ИСО 10993-13-99 Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 13. Идентификация и количественное определение продуктов градации полимерных материалов
3 Термины и определения
Общие термины
1 переднекамерная ИОЛ: ИОЛ, у которой оптический элемент и часть периферийного неоптического элемента находятся в передней камере.
2 заднекамерная ИОЛ для афакии: Заднекамерная ИОЛ, предназначенная для крепления в задней камере глаза при отсутствии естественного хрусталика.
3 заднекамерная ИОЛ для факичного глаза: Заднекамерная ИОЛ для крепления в задней камере глаза между радужкой и хрусталиком.
4 жесткая ИОЛ: ИОЛ с оптической частью, не предназначенной для складывания при имплантации.
5 мягкая ИОЛ: ИОЛ с оптической частью, предусматривающей возможность складывания при имплантации.
6 гидрогелевая ИОЛ: влагосодержащая ИОЛ, изготовленная из гидрогеля.
7 комбинированная ИОЛ: ИОЛ, отдельные элементы которой соответствуют определениям, приведенным в пунктах 4-6.
8 положительная ИОЛ: Модель ИОЛ, предназначенная для коррекции афакии или гиперметропии.
9 отрицательная ИОЛ: Модель ИОЛ, предназначенная для коррекции миопии.
10 монофокальная ИОЛ: Модель ИОЛ, имеющая одно значение оптической силы.
11 мультифокальная ИОЛ: Модель ИОЛ, имеющая более одного значения оптической силы.
12 сборная ИОЛ: ИОЛ, изготовленная методом сборки из отдельных элементов.
13 монолитная ИОЛ: ИОЛ, изготовленная из единого куска материала.
14 торическая ИОЛ: ИОЛ, имеющая оптическую поверхность с торической образующей.
15 элементы ИОЛ: Части ИОЛ, выполняющие различные функции.
16 оптический элемент: Часть ИОЛ, формирующая изображение; в общем случае - центральная.
17 тело: Центральная часть ИОЛ, включающая оптический элемент, непосредственно граничащая с опорной частью ИОЛ.
18 гаптика: Опорная, не оптическая часть ИОЛ, в общем случае - периферическая, выполняющая функцию крепления ИОЛ в определенном месте глаза.
19 гаптический элемент: Составная часть гаптики, изготавливаемая в различных вариантах: разомкнутая (дуга), замкнутая (петля) и т.п.
20 общий диаметр: Диаметр окружности, проходящей через максимально удаленные друг от друга точки гаптики.
21 фактор оптического профиля: Показатель, описывающий кривизну преломляющих поверхностей оптического элемента (плоско-выпуклая, двояковыпуклая и т.п.).
22 биологическая совместимость: Способность имплантата не вызывать ответной реакции организма, которая может повлечь воспалительные реакции.
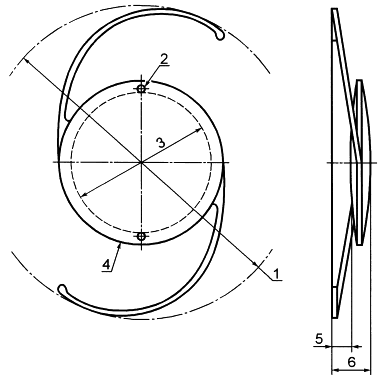
23 оптическая часть: Диаметр окружности с центром на оптической оси ИОЛ, обводящей только части ИОЛ, принадлежащие к оптической конструкции (рисунок 1).
1 - общий диаметр; 2 - позиционное отверстие; 3 - оптическая часть; 4 - тело; 5 - высота свода; 6 - саггиталь
Рисунок 1 - Схема ИОЛ
24 in situ: В равновесии с внутриглазной жидкостью при температуре плюс 35 °С.
Примечания
1 Показатель преломления внутриглазной жидкости принят равным 1,336 для длины волны 546,07 нм.
2 При испытаниях в качестве заменителя внутриглазной жидкости допускается использовать физиологический раствор.
3 Испытания допускается проводить в других условиях, если результаты испытаний соответствуют требованиям для условий in situ.
25 петля: Периферическое расширение тела, служащее для закрепления линзы внутри глаза.
Примечание - Петля является частью гаптики или может ее образовывать.
26 мультикомпонентная ИОЛ: ИОЛ, состоящая из отдельных компонентов - тела и петель.
Примечание - ИОЛ, состоящую из тела и двух петель, называют ИОЛ из трех частей.
27 однокомпонентная ИОЛ: ИОЛ, у которой гаптика и тело являются одним целым.
Термины, описывающие оптические свойства ИОЛ и методы их испытаний
28 задняя вершинная рефракция: Обратное значение приведенного параксиального фокусного расстояния in situ для света с длиной волны 546,07 нм.
Примечание - Единица измерения задней вершинной рефракции - обратные метры (м). Наименование данной единицы измерения "диоптрия", условное обозначение - дптр.
29 параксиальное фокусное расстояние: Расстояние между задней главной плоскостью и задней параксиальной фокальной точкой.
30 приведенное фокусное расстояние: Фокусное расстояние, деленное на показатель преломления окружающей среды.
Термины, описывающие механические свойства ИОЛ и методы их испытаний
31 оптическая децентрация: Горизонтальное смещение оптической части из-за сжатия гаптической(их) части(ей), составляющее расстояние между геометрическим центром чистой оптики и центром цилиндра заданного диаметра, в который заключена ИОЛ.
32 оптический наклон: Угол между оптической осью интраокулярной линзы в несжатом состоянии и в сжатом состоянии, когда ИОЛ заключена в цилиндр заданного диаметра.
33 сагитталь: Максимальное расстояние между плоскостями, перпендикулярными к оптической оси, которые проходят через крайние передние или крайние задние точки оптической части или гаптики ИОЛ (см. рисунок 1).
34 высота свода: Расстояние между плоскостью, перпендикулярной к оптической оси, проходящей через вершину ближайшей к радужке глаза оптической поверхности, и плоскостью, перпендикулярной к оптической оси, проходящей через ближайшую к радужке глаза точку несжатой гаптической части интраокулярной линзы (см. рисунок 1).
Примечания
1 Ближайшую к радужке глаза сторону ИОЛ определяют по ее расположению в имплантированном состоянии.
2 Высоту свода считают положительной, если расстояние определяется в направлении к сетчатке глаза, и отрицательной в обратном случае.
Термины, относящиеся к маркировке и упаковке
35 дополнительная упаковка: Контейнер, используемый в дополнение к основной упаковке для поддержания стерильности ИОЛ.
36 индивидуальное изделие: Медицинское изделие, изготовленное в соответствии с рецептом, выписанным должным образом подготовленным медицинским специалистом, специфические характеристики конструкции которого предназначены для использования этого изделия конкретным пациентом.
Примечание - Медицинские изделия массового производства, которые подвергаются дополнительной обработке для соответствия требованиям медицинского специалиста, не являются индивидуальными изделиями.
37 изделие для клинических испытаний: Изделие, предназначенное для использования должным образом подготовленным медицинским специалистом при проведении клинических испытаний.
38 изготовитель: Физическое или юридическое лицо, которое несет ответственность за конструирование, производство, упаковку и идентификацию медицинского изделия перед поставкой на рынок под торговой маркой, независимо от того, проводятся ли данные операции им лично либо от его имени другим лицом.
Примечание - Обязательства, которые берет на себя изготовитель, также относятся к физическому или юридическому лицу, которое производит сборку, упаковку, обработку, полную переработку и/или идентификацию изделия с целью поставки на рынок под его торговой маркой.
39 основная упаковка: Контейнер, который физически и напрямую защищает линзу и поддерживает ее стерильность.
40 самоклеящаяся этикетка: Этикетка, вкладываемая в упаковочный контейнер для использования в больничных записях.
41 упаковочный контейнер: Упаковка, предназначенная для защиты ИОЛ в процессе хранения и/или продажи.
Термины, относящиеся к биологической совместимости
42 испытание деградации материала: Испытание, которое определяет потенциал деградации материала.
43 испытание воздействием излучения Nd-YAG лазера: Испытание, по результатам которого определяют физические и химические эффекты, возникающие вследствие воздействия излучения Nd-YAG лазера на исследуемый материал.
44 испытание неокулярной имплантацией: Испытание, по результатам которого определяют локальную токсичность и раздражение, возникающие при воздействии на неокулярные ткани тестовым материалом и/или экстрактом из него, с использованием соответствующего места имплантации на животном.
45 испытание окулярной имплантацией: Испытание, по результатам которого определяют эффект локальной токсичности для окулярной ткани на микроскопическом и макроскопическом уровнях от исследуемого материала, который хирургически имплантирован в передний отрезок глаза животного.
46 испытуемый материал: Стерильная ИОЛ, предназначенная для имплантации человеку, или идентичный материал, изготовленный и обработанный в соответствии с утвержденной процедурой, эквивалентной используемой для производства ИОЛ.
Примечание - При использовании ИОЛ в качестве испытуемого материала предпочтительно использовать линзы с оптической силой от 18 до 22 дптр.
47 испытание фотостабильности: Испытание, по результатам которого определяют потенциал вырождения материала при облучении светом.
Термины, относящиеся к хранению и транспортированию
48 дата окончания срока годности: Дата, после которой ИОЛ не допускается использовать.
49 целостность упаковки: Способность контейнера сохранять ИОЛ от загрязнения в процессе транспортирования и/или хранения.
50 срок годности: Период, в течение которого ИОЛ считают годной для имплантации.
51 стабильность: Способность ИОЛ сохранять свойства и характеристики в пределах, указанных изготовителем, в течение срока годности.
Термины, относящиеся к клиническим испытаниям
52 предпочтительный субъект: Субъект, у которого отсутствует преоперативная патология.
53 совокупные неблагоприятные результаты: Общее число неблагоприятных результатов, которые произошли в любое время до заданного момента после операции.
54 модель ИОЛ: ИОЛ с совокупностью характеристик, определяемых методом изготовления и конструктивными особенностями ИОЛ.
Примечания
1 Примерами конструктивных особенностей ИОЛ являются: диаметр тела, оптический диаметр, фактор оптического профиля; примерами особенностей петель являются конфигурация, размер, угол.
2 Любое существенное изменение в применяемых для изготовления ИОЛ материалах (включая их состав и процесс синтеза) рассматривается как изменение модели ИОЛ.
55 базовая модель ИОЛ: Модель ИОЛ, которая признана годной на основании клинических испытаний не менее 100 субъектов и которая соответствует требованиям настоящего стандарта, ГОСТ Р ИСО 10993.1, ГОСТ Р ИСО 10993.5, ГОСТ Р ИСО 10993.6, ГОСТ Р ИСО 10993.10*, ГОСТ Р ИСО 10993.10*, [1]-[7].
_______________
* Соответствует оригиналу (повтор). - .
56 модификация уровня А базовой модели ИОЛ: Модификация базовой модели, которая признана незначительной и не может привести к ухудшению безопасности или потере эффективности по сравнению с базовой моделью ИОЛ.
57 модификация уровня В базовой модели ИОЛ: Модификация базовой модели, отличающаяся от модификации уровня А, указанной в пункте 56.
Примечание - Модификация уровня В может представлять угрозу для безопасности или эффективности ИОЛ, что приводит к существенному отличию модифицированной модели от базовой модели.
58 не доведенный до конца: Субъект с просроченным послеоперационным отчетом, с которым невозможно было связаться путем большого количества писем и телефонных звонков для определения окончательного клинического исхода.
Примечание - Данное определение не относится к умершим субъектам.
59 постоянный неблагоприятный исход: Неблагоприятный исход, который представлен в заключении о клинических испытаниях.
Алфавитный указатель терминов
Высота свода | 34 |
Гаптика | 18 |
Дата окончания срока годности | 48 |
Децентрация оптическая | 31 |
Диаметр общий | 20 |
Изготовитель | 38 |
Изделие для клинических испытаний | 37 |
Изделие индивидуальное | 36 |
In situ | 24 |
ИОЛ гидрогелевая | 6 |
ИОЛ жесткая | 4 |
ИОЛ заднекамерная для афакии | 2 |
ИОЛ заднекамерная для факичного глаза | 3 |
ИОЛ комбинированная | 7 |
ИОЛ монолитная | 13 |
ИОЛ монофокальная | 10 |
ИОЛ мультикомпонентная | 26 |
ИОЛ мультифокальная | 11 |
ИОЛ мягкая | 5 |
ИОЛ однокомпонентная | 27 |
ИОЛ отрицательная | 9 |
ИОЛ переднекамерная | 1 |
ИОЛ положительная | 8 |
ИОЛ сборная | 12 |
ИОЛ торическая | 14 |
Исход постоянный неблагоприятный | 59 |
Испытание воздействием излучения Nd-YAG лазера | 43 |
Испытание деградации материала | 42 |
Испытание неокулярной имплантацией | 44 |
Испытание окулярной имплантацией | 45 |
Испытание фотостабильности | 47 |
Контейнер упаковочный | 41 |
Материал испытуемый | 46 |
Модель ИОЛ | 54 |
Модель ИОЛ базовая | 55 |
Модификация уровня А базовой модели ИОЛ | 56 |
Модификация уровня В базовой модели ИОЛ | 57 |
Наклон оптический | 32 |
Не доведенный до конца | 58 |
Петля | 25 |
Расстояние параксиальное фокусное | 29 |
Расстояние приведенное фокусное | 30 |
Результаты совокупные неблагоприятные | 53 |
Рефракция задняя вершинная | 28 |
Сагитталь | 33 |
Совместимость биологическая | 22 |
Срок годности | 50 |
Стабильность | 51 |
Субъект предпочтительный | 52 |
Тело | 17 |
Упаковка дополнительная | 35 |
Упаковка основная | 39 |
Фактор оптического профиля | 21 |
Целостность упаковки | 49 |
Часть оптическая | 23 |
Элемент гаптический | 19 |
Элемент оптический | 16 |
Элементы ИОЛ | 15 |
Этикетка самоклеящаяся | 40 |
ПРИЛОЖЕНИЕ А
(справочное)
Библиография
[1] | ИСО 11979-2-1999 Имплантаты офтальмологические. Интраокулярные линзы. Часть 2. Оптические свойства и методы испытаний |
[2] | ИСО 11979-3-1999 Имплантаты офтальмологические. Интраокулярные линзы. Часть 3. Механические свойства и методы испытаний |
[3] | ИСО 11979-4-1999 Имплантаты офтальмологические. Интраокулярные линзы. Часть 4. Информация на этикетках |
[4] | ИСО 11979-5-2000 Имплантаты офтальмологические. Интраокулярные линзы. Часть 5. Биологическая совместимость |
[5] | ИСО 11979-6-2000 Имплантаты офтальмологические. Интраокулярные линзы. Часть 6. Срок годности и стабильность при транспортировании |
[6] | ИСО 11979-7-1999 Имплантаты офтальмологические. Интраокулярные линзы. Часть 7. Клинические испытания |
[7] | ИСО 11979-8-2000 Имплантаты офтальмологические. Интраокулярные линзы. Часть 8. Общие требования |
Электронный текст документа
и сверен по:
М.: ИПК Издательство стандартов, 2002